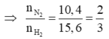Hỗn hợp X gồm N2 và H2 có tỉ khối so với H2 là 6,2 . Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y . Khối lượng mol của Y là ?

Những câu hỏi liên quan
Hỗn hợp X gồm N2 và H2 có tỉ khối so với hiđro là 6,2. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. có giá trị là : A. 14,76 B. 18,23 C. 7,38 D. 13,48
Đọc tiếp
Hỗn hợp X gồm N2 và H2 có tỉ khối so với hiđro là 6,2. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. có giá trị là :
A. 14,76
B. 18,23
C. 7,38
D. 13,48
Hỗn hợp X gồm N2 và H2 có tỉ khối so với hiđro là 6,2. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. có giá trị là A. 14,76 B. 18,23 C. 7,38 D. 13,48
Đọc tiếp
Hỗn hợp X gồm N2 và H2 có tỉ khối so với hiđro là 6,2. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. có giá trị là
A. 14,76
B. 18,23
C. 7,38
D. 13,48
Đáp án C
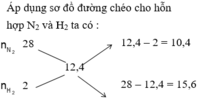
Áp dụng sơ đồ đường chéo cho hỗn hợp N2 và H2 ta có : n N 2 n H 2 = 2 3
=> H2 thiếu, hiệu suất phản ứng tính theo H2.
Chọn n N 2 = 2 m o l n H 2 = 3 m o l
nH2 pư = 3 . 40% = 1,2 mol,
n N2 phản ứng = 0,4 mol
n NH3 sinh ra =0,8 mol.
n Y = n X - 0 , 8 = 2 + 3 - 0 , 8 = 4 , 2 m o l
Bảo toàn khối lượng :
![]()
Vậy tỉ khối của Y với H2 là 7,38
Đúng 0
Bình luận (0)
Hỗn hợp X gồm N2 và H2 có
M
x
12
,
4
. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y.
M
y
có giá trị là: A. 15,12 B. 18,23 C. 14,76 D. 13,48
Đọc tiếp
Hỗn hợp X gồm N2 và H2 có M x = 12 , 4 . Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. M y có giá trị là:
A. 15,12
B. 18,23
C. 14,76
D. 13,48
Hỗn hợp X gồm
N
2
v
à
H
2
có
n
H
2
0
,
4
m
o
l
;
A
l
→
A
l
3
+
+
3
e
;
M
g...
Đọc tiếp
Hỗn hợp X gồm N 2 v à H 2 có n H 2 = 0 , 4 m o l ; A l → A l 3 + + 3 e ; M g → M g 2 + + 2 e . Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết hiệu suất tổng hợp N H 3 đạt 40% thì thu được hỗn hợp Y. có giá trị là :
A. 15,12
B.18,23
C.14,76
D.13,48
Chọn C
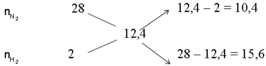
Áp dụng sơ đồ đường chéo cho hỗn hợp N2 và H2 ta có :
![]()
Với tỉ lệ trên suy ra H2 thiếu, hiệu suất phản ứng tính theo H2.
Trong hỗn hợp X ta chọn n N 2 = 2 n H 2 = 3
Số mol H2 phản ứng là 3.40% = 1,2 mol, suy ra số mol N2 phản ứng là 0,4 mol, số mol NH3 sinh ra là 0,8 mol. Sau phản ứng số mol khí giảm là (1,2 + 0,4) – 0,8 = 0,8 mol.
Sau phản ứng số mol khí giảm là 0,8 mol nên : n Y = n x − 0 , 8 = 2 + 3 − 0 , 8 = 4 , 2 mol
Theo định luật bảo toàn khối lượng ta có : m Y = m x = m N 2 + m H 2 = 2 . 28 + 3 . 2 = 62 gam
Vậy M ¯ Y = m Y n Y = 62 4 , 2 = 14 , 76
Đúng 0
Bình luận (0)
Hỗn hợp X gồm
N
2
và
H
2
có
M
X
12
,
4
. Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết hiệu suất tổng hợp
NH
3
đạt 40% thì thu được hỗn hợp Y.
M
Y
có giá trị là : A.15,12 B.18,23 C.14,76 D.13,48
Đọc tiếp
Hỗn hợp X gồm N 2 và H 2 có M X = 12 , 4 . Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết hiệu suất tổng hợp NH 3 đạt 40% thì thu được hỗn hợp Y. M Y có giá trị là :
A.15,12
B.18,23
C.14,76
D.13,48
Hỗn hợp X gồm N2 và H2 có \(\overline{M_{tb}}=12,4\) Dẫn X đi qua bình đựng bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y.\(\overline{M_y}\) có giá trị là.Giải chi tiết giúp mình nha.
Hỗn hợp X gồm N2 và H2 có overline{M_x}12,4. Dẫn X đi qua bình đựng bột Fe rồi nung nóng ( hiệu suất tổng hợp NH3 đạt 40%) thu được hỗn hợp Y. overline{M_y} có giá trị là( không giải phương pháp giải bằng sơ đồ đường chéo nha mọi người ! )
Đọc tiếp
Hỗn hợp X gồm N2 và H2 có \(\overline{M_x}=12,4\). Dẫn X đi qua bình đựng bột Fe rồi nung nóng ( hiệu suất tổng hợp NH3 đạt 40%) thu được hỗn hợp Y. \(\overline{M_y}\) có giá trị là
( không giải phương pháp giải bằng sơ đồ đường chéo nha mọi người ! )
Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{H_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{28x+2y}{x+y}=12,4\)
\(\Leftrightarrow12,4x+12,4y-28x-2y=0\Leftrightarrow-15,6x=-10,4y\\ \Leftrightarrow\dfrac{x}{y}=-\dfrac{10,4}{-15,6}=\dfrac{2}{3}\)
Giả sử \(\left\{{}\begin{matrix}n_{N_2}=2\left(mol\right)\\n_{H_2}=3\left(mol\right)\end{matrix}\right.\)
\(n_{khí.giảm}=n_{NH_3}=\dfrac{2}{3}n_{H_2}.H\%=\dfrac{2}{3}.3.40\%=0,8\left(mol\right)\)
\(n_Y=2+3-0,8=4,2\left(mol\right)\)
\(m_Y=m_X=28.2+2.3=62\left(g\right)\)
\(\overline{M_Y}=\dfrac{62}{4,2}=14,76g/mol\)
Đúng 2
Bình luận (0)
\(n_{N_2}=a;n_{H_2}=b\\ PT:\dfrac{1}{2}N_2+\dfrac{3}{2}H_2-Fe,t^{^0}->NH_3\\ M_X=\dfrac{28a+2b}{a+b}=12,4\\ a=1,5b\\ Sau.pư:\\ M_Y=\dfrac{2.0,6b+28\left(a-\dfrac{0,4b}{3}\right)+17.0,4b}{0,6b+a-\dfrac{0,4b}{3}+0,4b}=19,55\)
Đúng 1
Bình luận (0)
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là A. 36% B. 25% C. 50% D. 40%
Đọc tiếp
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 36%
B. 25%
C. 50%
D. 40%
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là A. 36%. B. 25%. C. 50%. D. 40%.
Đọc tiếp
Hỗn hợp khí X gồm N2 và H2 có tỉ khối so với H2 là 3,6. Nung nóng X một thời gian trong bình kín (có bột Fe làm xúc tác), thu được hỗn hợp khí Y có tỉ khối đối với H2 là 4. Hiệu suất của phản ứng tổng hợp NH3 là
A. 36%.
B. 25%.
C. 50%.
D. 40%.
Đáp án B
Hỗn hợp ban đầu chứa N 2 : 0 , 2 H 2 : 0 , 8
→ Hiệu suất tính theo N2.
nsau = 3,6/4 = 0,9 → N2 phản ứng = 0,05 → H = 25%
Đúng 0
Bình luận (0)